

Беседа Бориса Штерна с докт. биол. наук, научн. сотр. Оснабрюкского университета (Германия) Арменом Мулкиджаняном о происхождении, распространении жизни и о том, как бактерии научились использовать кислород. Видеоверсия интервью: youtu.be/URdKc16JTa8. Другие беседы «Место жизни во Вселенной»: trv-science.ru/tag/proisxozhdenie-zhizni.
— Здравствуйте! Сегодня у нас снова Армен Мулкиджанян и разговор вновь пойдет о происхождении жизни. Вернее, сейчас не просто о жизни, а о ее мощнейшем геологическом результате — кислородной атмосфере. Напомню: в прошлом интервью с Евгением Куниным о происхождении эукариот 1 было четко сказано, что без предшествующей подготовки, главной составляющей которой был кислород, развитая жизнь не смогла бы появиться вообще. Эукариоты появились только после так называемой кислородной катастрофы (Great Oxidation Event), на подготовку которой ушло больше миллиарда лет: сначала возник кислородный фотосинтез, затем какие-то первые признаки кислорода… Об этом мы сегодня и будем говорить. Давайте c самого начала. Армен, вам слово.
— Спасибо. Прежде чем приступить к кислородному фотосинтезу, нам надо понять, что такое фотосинтез вообще. Это процесс, при котором живые организмы — не все, а избранные, фотосинтезирующие, — ловят кванты видимого света и используют их для получения сахаров (в самом грубом смысле). Мы — живые организмы — построены из органических молекул, которых в неживой природе очень мало. Имеет смысл обсудить, как так получилось. Чем органические молекулы отличаются от неорганических? Тем, что органические молекулы содержат атомы углерода, связанные с атомами водорода, т. е. эти молекулы восстановлены. В неорганической природе углерод существует в основном как диоксид углерода — тот самый СО2, с которым мы зачем-то боремся. А живые организмы берут этот СО2 из атмосферы или воды и дальше передают каким-то образом два электрона на этот СО2, и эти отрицательные электроны захватывают те самые нужные, положительно заряженные ионы водорода, протоны, всегда присутствующие в воде, и из СО2 получается муравьиная кислота. При переносе еще двух пар электронов получается метиловый спирт, который не надо пить, а потом, в конце концов, получается метан.
И фокус в том, что электроны, которые надо забросить на углерод, чтобы его восстановить, должны иметь большой отрицательный окислительно-восстановительный потенциал (очень большую восстановительную силу, если по-простому). Чем выше восстановительная сила, тем ниже значения окислительно-восстановительного потенциала, он же редокс-потенциал. Если мы возьмем какое-то вещество с редокс-потенциалом, достаточно низким для восстановления CO2, и, например, попробуем им восстановить воду, то у нас это получится, ведь в воде есть протоны, которые примут эти электроны — их даже проще восстановить, чем CO2. При этом образуется молекула водорода в результате разложения воды. Таким образом, процесс образования органических веществ требует столь сильных восстановителей, которые даже разлагают воду.
Это важно знать, потому что если у вас есть водный раствор, в котором плавает, условно говоря, СО2, то восстановить этот диоксид углерода сложно, так как протоны воды будут забирать эти электроны и СО2 не будет восстанавливаться, даже если у вас есть сильный восстановитель.
Тут возникает куча разных проблем, и эти проблемы эволюция как-то решила: в какой-то момент возникли достаточно сложные организмы, которые научились, несмотря на перечисленные трудности, восстанавливать CO2. Это произошло явно не сразу. В самом начале на Земле была немножко другая геология, и вот эти органические вещества образовывались в больших количествах сами по себе, есть все основания так считать. А потом геология изменилась и производство органики упало. Но к этому времени уже была какая-то жизнь — она и создала системы восстановления CO2 до органических молекул. Способность восстанавливать CO2 до органических молекул называется автотрофией: автотрофным организмам еда не нужна, вернее, они могут делать ее из воздуха. И белковые комплексы, которые всё это делают, — они и есть самые сложные их тех, что существуют в живых организмах. Таких систем несколько, с десяток; фотосинтез — лишь одна из таких систем, добывающих разными хитростями эти обладающие очень сильной восстановительной силой электроны. Фотосинтез — самая мощная из этих систем, так как она использует энергию солнечного света. Солнечного света много, и поэтому 90–95% органики на Земле (не знаю точно) образуется в результате фотосинтеза.

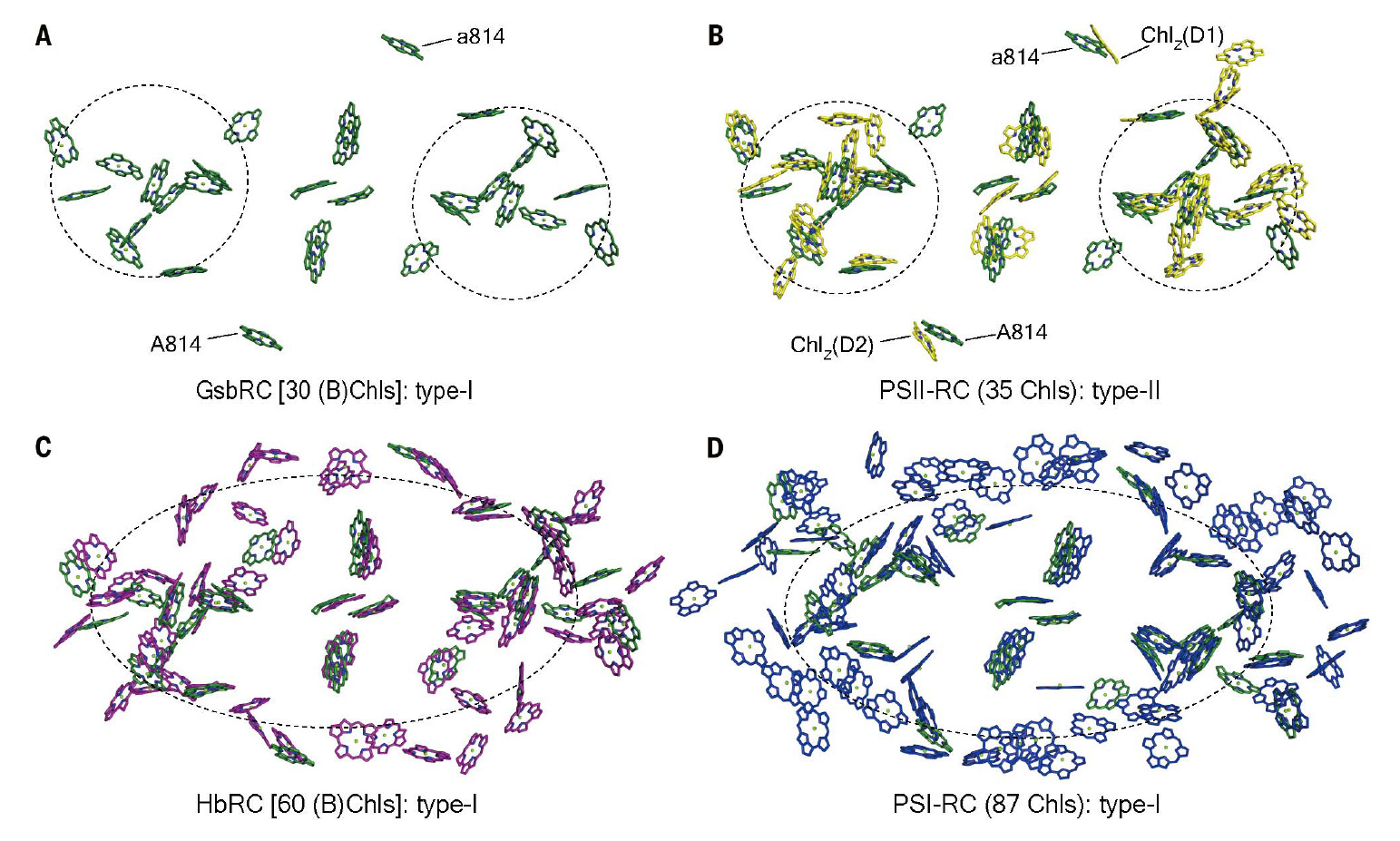
Для фотосинтеза нужна специальная фотосинтетическая мембрана. Для самых простейших способных к фотосинтезу бактерий эту функцию выполняет мембрана, окружающая их клетки. Дальше возникают некие усложнения: организмам для увеличения количества фотосинтетических ферментов хорошо бы иметь внутриклеточные плотно упакованные мембраны, чтобы фотосинтеза было больше; они есть у некоторых бактерий. В эти мембраны встроены сложные белковые комплексы, содержащие много молекул хлорофилла или бактериохлорофилла (рис. 1). В середине такого комплекса находятся две молекулы хлорофилла, которые образуют своеобразный бутерброд, сэндвич. Когда эта парочка немного смещенных друг от друга молекул ловит квант света, происходит разделение зарядов: на одной молекуле остается электрический плюс, а на другой — минус. Квант света сам по себе нейтральный, это фотон. Но за счет такой сэндвичной структуры происходит разделение на плюс-минус. Минус — это электрон; оказавшись на молекуле хлорофилла он превращает ее в очень сильный восстановитель с очень низким редокс-потенциалом — меньше минус одного вольта (–1 В). Это очень много и вполне достаточно, чтобы восстановить углекислоту, но процесс происходит непрямо: электрон долго путешествует внутри комплекса, так как плюс и минус надо очень быстро оттащить друг от друга, чтобы те не схлопнулись, а на это тратится часть энергии. Путешествует электрон по способным к быстрому окислению и восстановлению редокс-группам в этих белках. В конце концов этот электрон застревает на определенной группе, у которой всё еще очень низкий потенциал, и оттуда он может уйти в какие-то химические реакции, в результате них в конечном счете восстановится CO2. Таким образом, процесс достаточно сложный: происходит разделение зарядов, электрон быстро уносится поперек мембраны на расстояние 25–27 ангстрем, чтобы не вернулся, и дальше там он участвует в каких-то химических реакциях. Так и образуются органические молекулы.
Что важно, так это то, что у нас на сэндвиче из двух молекул хлорофилла остается плюс — электронная вакансия, дырка, которую нельзя оставлять пустой. И вот, собственно, эволюционная часть истории — это про то, чем заполнялась эта дырка в ходе эволюции. Проблема затыкания дырки очень важная, потому что электроны с образованием органики, сахаров, теряются необратимо, а фотосинтез должен работать, для чего дырку как-то надо заполнять…
Тут можно кое-что рассказать по этому поводу. Белковые комплексы, о которых идет речь, называются фотохимическими реакционными центрами (ФРЦ). Они бывают двух типов — первого и второго. Почему так? Потому что у зеленых растений этих центров два. Они разные и работают по цепочке. Электроны с первого ФРЦ идут не куда-то в метаболизм, а на второй центр, где вновь происходит разделение зарядов (рис. 2). То есть у нас электрон пробегает через два ФРЦ, так что у зеленых растений самый сложный фотосинтез. Поэтому фотореакционные центры организмов, имеющих только один такой центр, относят либо к первому, либо ко второму типу по степени их похожести на первую или вторую фотосистему зеленых растений.

Как эти два типа фотореакционных центров между собой соотносятся, до недавнего времени сказать было сложно, хотя очень отдаленное сходство между первой и второй фотосистемами зеленых растений отмечалось. Относительно недавно ситуация несколько прояснилась; удалось получить структуры всех известных видов бактериальных ФРЦ.
Вообще говоря, структуры белков получают давно, еще с 1950-х годов, используя рентгеноструктурный анализ кристаллов белка. Образуемые белками кристаллы освещают пучком рентгеновских лучей, лучи рассеиваются, и по этой дифракционной картине восстанавливается структура. Фокус в том, что белки надо для этого сперва кристаллизовать. А вот мембранные белки — они снаружи «жирные», так как внутренний слой биологических мембран образован гидрофобными частями жирных кислот. Поэтому мембранные белки снаружи покрыты «жирными» химическими группами, чтобы взаимодействовать с «жирной» мембраной. Такие белки кристаллизоваться не хотят.
Так что структур разных белков наполучали много, сотни тысяч, но это были где-то на 98–99% водорастворимые белки. Мембранные белки очень долгое время кристаллизовать вообще не получалось. Впервые это удалось в 1984 году, и за это дали Нобелевскую премию немецким ученым Хартмуту Михелю, Иоганну Дайзенхоферу и Роберту Хуберу. А следующий, другой «жирный» мембранный белок закристаллизовали только в 1995 году, так что в течение 11 лет был только один мембранный белок с известной структурой, и это был как раз ФРЦ из протеобактерий. И поэтому очень много народу, в том числе и мы, исследовали этот ФРЦ; в этой ситуации ты имеешь структуру, а зная ее, можно ставить более осмысленные опыты. За это десятилетие интенсивных исследований про устройство фотосинтеза удалось узнать достаточно много.
В структурной же биологии за последние десять лет случился колоссальный прорыв: сейчас можно получать структуры любых белков, прибегая к криоэлектронной микроскопии. Этот метод заключается в том, что сначала образец белка замораживается, а дальше с помощью неких хитростей и хорошего электронного микроскопа уже можно определить его структуру. И этому методу совершенно всё равно, с каким белком работать, с мембранным или с водорастворимым, с большим или маленьким. Поэтому сейчас выходит много статей со структурами мембранных белков. Я всю жизнь занимался мембранными белками, их структур было очень мало. А сейчас вот они пошли…
И вот считается, что древние фотосинтезирующие организмы сперва отбирали электроны у сернистых соединений, т. е. окисляли их. Эти фотосинтезирующие организмы достаточно давно возникли — нужно же было как-то делать органику, когда ее абиотическое производство затухло. И дальше фотосинтезирующие организмы всё время окисляли природу вокруг: жили, например, в водоеме, и вся сера, какая там была, окислялась.
Что было делать дальше? Дальше считается (опять же более-менее гипотетически, но с весомыми основаниями), что вот в этом древнем водоеме, когда кислорода еще не было, имелось достаточно много железа. Катионы двухвалентного железа (Fe2+) более-менее прилично растворяются в воде, и водоемы были железистыми. И считается, что эти древние ФРЦ, окислив всю серу, стали окислялять Fe2+. Они могли это делать, потому что редокс-потенциал образующейся в ФРЦ дырки достаточно высокий, можно было даже у Fe2+ оторвать электрон с образованием трехвалентного железа, нерастворимые окиси и соли которого выпадали на дно. В старых породах, которым от 3,8 млрд лет, находят перемежающиеся слои двух- и трехвалентного железа — считают, что оно возникло в результате фотосинтеза. Когда фотосинтез был активный, отлагалось много трехвалентного железа, потом, например, наступала какая-то глобальная зима, фотосинтез заканчивался, водоемы покрывались льдом, и тогда откладывалось только двухвалентное железо; впоследствии опять фотосинтез активировался, и появлялось вновь трехвалентное железо.
Я помню, что по крайней мере двадцать лет назад были сообщения об открытии больших отложений трехвалентного марганца. Тогда была высказана идея, что когда железо всё окислилось, то фотосинтезирующие организмы начали окислять растворенные ионы двухвалентного марганца — это проходит по величинам редокс-потенциала, это возможно. Но, видимо, двухвалентный марганец тоже когда-то кончился. И тогда возникли организмы уже более сложные, которые научились окислять воду, забирая у нее электроны. Воды много, она никогда не кончится. В каталитическом сайте такого окисляющего воду ФРЦ связываются две молекулы воды. От них по одному отбираются электроны. И когда отбирается четвертый электрон, происходит некая реакция, при которой два кислорода О от воды объединяются с образованием О2. Это молекулы кислорода. И высвобождается четыре протона. Эта молекула кислорода дальше уходит в воду или в атмосферу — куда получится. И весь кислород, который есть в атмосфере Земли, из этой фотохимической реакции и происходит.
Химически это очень нетривиальная реакция. Такой каталитический центр возник в эволюции только один раз. Он, соответственно, есть у зеленых растений — это фотосинтез, о котором мы знаем, — но на самом деле он возник не у них, а получили его зеленые растения от цианобактерий, которые люди иногда называют сине-зелеными водорослями. Они не водоросли; они, собственно говоря, бактерии.
Проблема в том, что редокс-потенциал, который нужен, чтобы отобрать электроны от воды, очень большой — гораздо больше одного вольта. И тогда энергии кванта света не хватает, чтобы забросить электрон до тех низких редокс-потенциалов, которые нужны, чтобы восстановить СО2 до органики. Поэтому фотосистема, разлагающая воду, всегда работает в тандеме с еще одной фотосистемой, которая берет эти электроны и вторым квантом света забрасывает их еще выше, откуда они потом переносятся на СО2.
Такой двухступенчатый механизм возник у бактерий около 2,7–3 млрд лет назад, а дальше, 1,5–2,5 млрд лет назад, возникли эукариотические клетки, о которых говорил Евгений Викторович Кунин. Они сперва возникли за счет симбиозов, о которых он рассказывал, а потом произошел еще один симбиоз уже сложившейся эукариотической клетки с цианобактерией. Эта цианобактерия превратилась в хлоропласт. И тогда эта клетка приобрела еще и возможность просто жить даром за счет фиксации СО2 светом, возникли растения. Такие симбиозы с фотосинтезирующими организмами происходили несколько раз. Хлоропласт имеет свой маленький геном. И по этим генам можно выяснить, на какие группы цианобактерий похожи хлоропласты. И, в общем, выясняется, что по меньшей мере два раза эукариотические организмы забирали разные виды цианобактерий, превращали в хлоропласты и заставляли на себя работать. Это независимо произошло, с одной стороны, у большинства растений, с другой — у красных водорослей. Помимо двух этих случаев, когда бывшие цианобактерии передали бо́льшую часть своих генов в хозяйский геном и стали хлоропластами, есть случаи, когда какие-то простейшие организмы просто ловят соседские цианобактерии или целые водоросли, держат их у себя — при этом захваченные организмы еще не успели измениться. Может, это начало какого-то будущего симбиоза, но пока это два отдельных организма. И вот водоросли живут внутри и просто фотосинтезируют, кормят хозяина. Вот такая история про кислородный фотосинтез.
— Можно вопрос по ходу? Каков порог фотосинтеза по энергии гамма-кванта? Вы сказали, если бы были фотоны несколько электронвольт (такие есть — это, вообще говоря, ультрафиолет), то дело могло бы идти в одну стадию. Какие кванты самые низкопороговые бактерии могут «хватать»?
— Фотосинтетические системы эволюционируют, и одно из направлений эволюции связано с тем, что фотосинтезирующие микроорганизмы жили и живут в этаких микробных матах: это такая губчатая слоистая структура из живущих друг над дружкой колоний разных бактерий; обычно наблюдается у берегов водоемов. Свет падает сверху, и фотосинтетические организмы, живущие сверху, ловят какую-то часть спектра, пропуская оставшийся свет к нижележащим слоям бактерий. И к тем фототрофным бактериям, которые ниже всех, свет, который ловится нормальным хлорофилом, не доходит. И тогда обделенные бактерии научаются ловить свет в других областях спектра. И вот эта эволюция шла таким образом, что спектр поглощения глубже живущих микроорганизмов, в частности, уходил в дальнюю красную область. При фотосинтезе зеленых растений листья поглощают синий и красный свет. Часть энергии синего света теряется за 10–15 с в тепло, использовать ее за это время не удается, и молекула хлорофилла «сваливается» на энергетический уровень, соответствующий поглощенному кванту красного света. Красный свет поглощается при 700 нм. Энергия этого кванта — 1,8 эВ. То есть зеленые растения используют, благодаря двум фотосистемам, два кванта примерно по 1,8 эВ каждый. А вот бактерии в нижних слоях мата могут поглощать свет с длиной волны до более 1000 нм, это инфракрасный, не видимый нами свет, и энергия его кванта где-то около 1,2 эВ. Более длинноволновых хлорофиллов я не знаю.

На этот вопрос я ответил?
— Да, продолжаем.
Собственно, об этом дальше и речь. Кислород, образующийся как побочный продукт разложения воды, — очень сильный окислитель, который может отобрать электроны, в общем-то, у всего, у любой органической молекулы. Хорошо известно, что где-то 2,4–2,5 млрд лет назад произошли изменения в соотношении изотопов серы в минералах, которые, по мнению геологов, говорят о том, что в этот период в атмосфере резко увеличилось количество кислорода. Кислород, который нарабатывали эти самые цианобактерии, с этого времени стал как бы задавать окислительно-восстановительный потенциал всей земной среды.
Сейчас много пишут о том, что, может быть, кислород начал генерироваться в фотосинтезе задолго до кислородной катастрофы, поскольку, образуясь, он окислял всё, что можно было легко окислить, — какие-то сернистые соединения, что-то из атмосферы… То есть исходно не происходило накопление кислорода, он сразу же употреблялся на окисление чего-нибудь. И вот в самые последние годы появлялись статьи, что этот процесс сам по себе мог занимать сотни миллионов лет, а вот 2,5 млрд лет назад произошел, что называется, облом, когда кислород окислил всё, что мог, и дальше стал накапливаться в атмосфере. Содержание кислорода в атмосфере достигает значения в 21%, а больше как-то не получается — видимо, такова термодинамика, окисление воды работает на пределе. То есть при дальнейшем повышении содержания кислорода в атмосфере реакция разложения воды идет в другую сторону — существует термодинамический предел. За счет энергии двух красных квантов света удается накачать 21% кислорода в атмосферу, а больше не получается. С этим и живем. 21% — это очень много, потому что О2 — это очень химически активное соединение, которое проникает повсюду. Вся дальнейшая эволюция после возникновения кислорода в той или иной степени сводилась к приспособлению разных организмов к кислороду в атмосфере.
Поскольку кислород всё окисляет, значит, надо как-то предотвращать окисление. Как это можно сделать? А давайте мы будем иметь не одну клетку, а многоклеточный, многослойный организм. Тогда кислород должен диффундировать, проникать через слои клеток. Пока он продиффундирует, его можно обезвредить, так что клетки в глубине и спасутся. Так и возникли многоклеточные организмы. Что еще можно придумать? Давайте когда вот эта молекула кислорода подойдет к внешней стороне бактериальной клетки, мы на нее набросимся и сделаем с ней что-нибудь химическое — например, превратим ее обратно в воду, накидав электронов, тогда она не сможет принести вред.
Такое явление и называется кислородным дыханием. Разные организмы дышат по-разному, и эффективность этого дыхания тоже разная. Дело в том, что за счет этого восстановления кислорода на внешней мембране можно еще и добывать энергию. Окисление разных веществ кислородом сопряжено с выделением энергии. Количество выделяющейся энергии зависит от природы окисляющегося кислородом вещества, а степень запасания этой энергии зависит от природы и сложности участвующих ферментов. Есть такое понятие, как «полная дыхательная цепь» — ею обладают организмы, способные запасти максимальное количество энергии из окисления органических молекул кислородом (рис. 4). Такие организмы отбирают электроны у своих органических кислот и отправляют их в долгий путь на кислород через большое количество разных мембранных комплексов; это очень сложная процедура. Такой перенос электронов связан с выделением большого количества энергии, потому что редокс-потенциал воды — +800 мВ, а отбирается всё это от органики, у которой редокс-потенциал –300 ÷ –400 мВ. Благодаря участию большого числа разный комплексов, больше одного электрон-вольта энергии забирается порциями и превращается в АТФ, энергетическую валюту клетки.
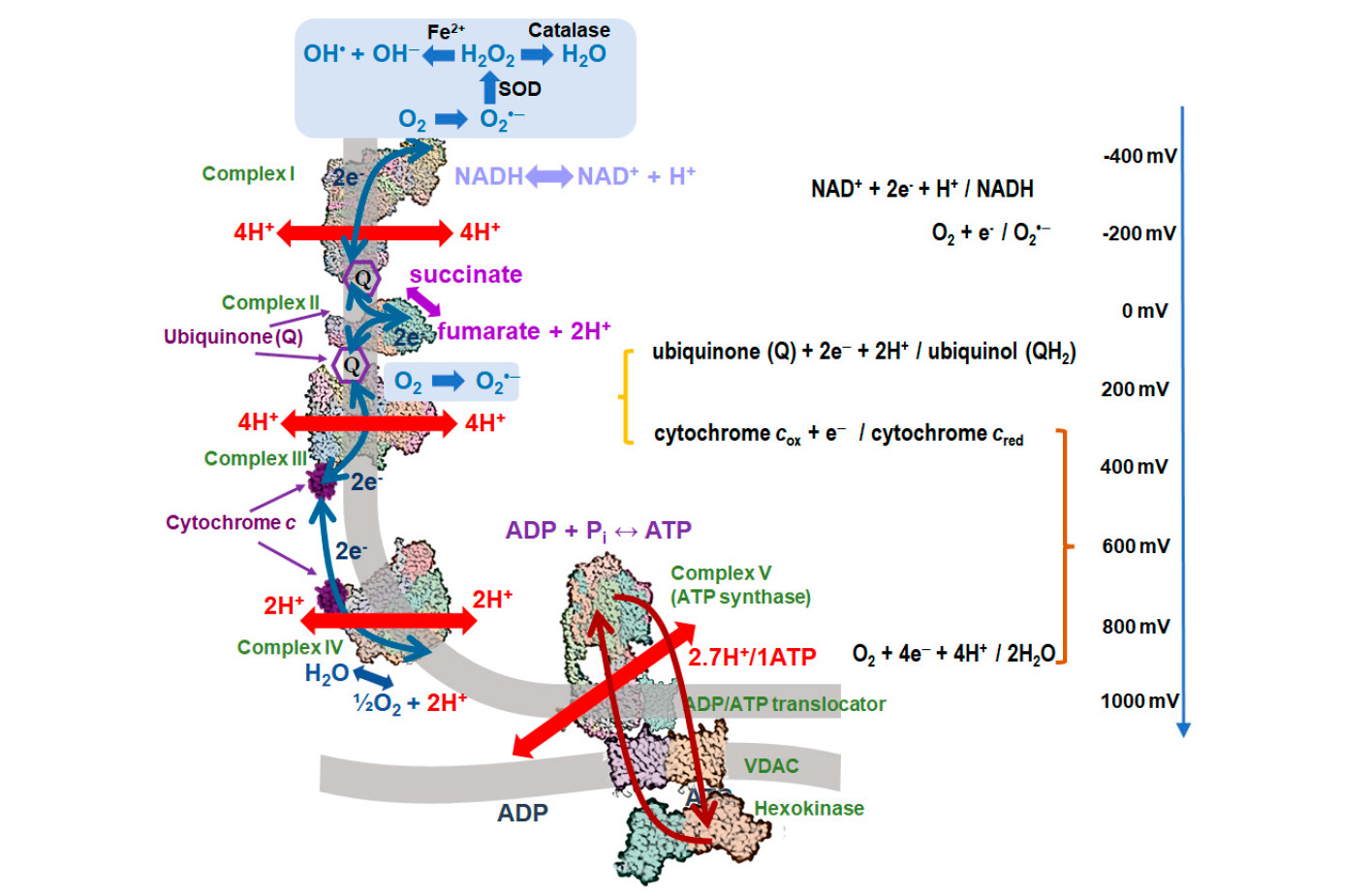
Skulachev V. P., Vyssokikh M. Y., Chernyak B. V., Mulkidjanian A. Y., Skulachev M. V., Shilovsky G. A., Lyamzaev K. G., Borisov V. B., Severin F. F., Sadovnichii V. A. Six Functions of Respiration: Isn’t It Time to Take Control over ROS Production in Mitochondria, and Aging Along with It? // Int. J. Mol. Sci. 2023, 24, 12540. doi.org/10.3390/ijms241612540
То есть из реакции окисления органики кислородом выжимается максимум в смысле синтеза АТФ для энергетических нужд, а заодно кислород восстанавливается до безвредной воды. Такая эффективная система сложно устроена. Исходно возникнув как система защиты от кислорода, дыхательная цепь усложнялась, собираясь из отдельных ферментных комплексов, которые до появления кислорода были задействованы в каких-то других клеточных процессах. Мы об этом писали 4, и вот сейчас еще вышел маленький обзорчик от американских коллег 5, которые придумали назвать этот эволюционный процесс бриколажем 6. Для каждого из ферментных комплексов дыхательной цепи можно проследить предысторию, а именно что он делал раньше и где. И вот некие бактерии, уже имеющие полную дыхательную цепь, в какой-то момент задружились с предшественником эукариотической клетки.
Опять же об этом говорил Кунин: много лет назад высказывались идеи, что эукариотическая клетка возникла в результате взаимодействия между какой-то архейной клеткой — представителем альтернативной бактериям группы (домена) безъядерных организмов — и дышащей бактерией. Архейная клетка заглотнула бактерию, и образовалась эукариотическая клетка. Уже тогда было понятно, что это очень упрощенная схема.
Так просто, скорее всего, не было, и то, что рассказывал Кунин, звучит гораздо более правдоподобно: видимо, симбиозов было несколько, и, видимо, были еще переносы каких-то групп генов, не связанные со слиянием различных организмов. То есть эта исходная, как ныне понятно, асгардархея (от которой эукариоты, а значит, и мы с вами, получили системы передачи геномной информации и синтеза белка) была, скорее всего, гетеротрофом, т. е. организмом, неспособным синтезировать органику из СО2 и зависящим от органики, произведенной где-то еще. Никакого фотосинтеза или хемосинтеза этот организм не осуществлял, а просто жрал, всё, что вокруг. Потому что ближайшие родственники эукариотических клеток — группа асгардархей — донные: живут на дне, ползают, что-то там едят… И они просто ели кого-то и по ходу этого дела, видимо, могли встраивать чужие гены себе в геном. По Кунину, их в некий момент тоже съели, но не переварили; а именно их заглотнула большая дельта-протеобактерия. Судя по особенностям эукариотических мембран, это могло произойти достаточно давно, скорее всего, еще до появления кислорода. Приобретение будущей митохондрии произошло существенно позже, и это, видимо, и был последний этап образования эукариотических клеток.
Процесс приобретения митохондрий тоже интересен, потому что у них тоже есть маленькие геномы. Когда посмотрели эти гены и поискали бактерий с похожими генами, нашли альфа-протеобактерии. Митохондрия — это бывшая альфа-протеобактерия. Причем среди альфа-протеобактерий ближайшими родственниками оказались бактерии, относящиеся к порядку Rickettsiales. Рикке́тсии — это бактерии, которые живут внутри клеток других организмов и вызывают у людей и у скота риккетсиозы — болезни, иногда смертельные. В последнее время выяснилось, почему такой вред от риккетсий человеку или скотине: они для риккетсий хозяева только промежуточные. У риккетсий сложный цикл развития, и их главный хозяин — членистоногие, например насекомые. С ними отношения другие, потому что если как-то исхитриться и лишить насекомых возможности заразиться «их» риккетсиями, то насекомые мрут — там, скорее всего, уже установился симбиоз, какая-то взаимозависимость между риккетсиями и клетками этих насекомых. То есть люди умирают от заражения риккетсиями, а насекомые, наоборот, умирают, если не заражены риккетсиями. То есть риккетсия может быть полезна хозяйской клетке. Нечто подобное, скорее всего, произошло и с предками эукариотической клетки. Другое дело, что все эти симбиозы, о которых я говорю, достаточно свежие, потому что эти самые членистоногие тоже возникли относительно недавно. А происхождение эукариотической клетки — это событие давнее, произошедшее где-то 1,5–2,5 млрд лет назад. Тогда, видимо, возник симбиоз между проэукариотической клеткой и риккетсией. Недавно вышла статья 7, про то, что что предками митохондрий были бактерии из отряда риккетсий, но не из семейства Rickettsiaсeae, а из иного семейства — Anaplasmataceae. От них, видимо, и происходят митохондрии.
В любом случае симбиоз оказался очень выгодным и сохранился в дальнейшем. И за счет этого эукариоты, которые сдружились с этой альфа-бактерией, выжили. Потому что у нас нет ни безмитохондриальных эукариот, ни чего-то, похожего на описанного Куниным и соавторами проэукариота — химеры из асгардархеи и дельта-протеобактерии. Произошла кислородная катастрофа, и все эти промежуточные формы вымерли, остались только полноценные эукариоты, за которых выдышивали кислород живущие в них митохондрии, бывшие альфа-протеобактерии. Поскольку митохондрии всё время потребляют кислород, его концентрация внутри эукариотической клетки достаточно низкая.
При этом, обладая полной дыхательной цепью, эта бывшая альфа-протеобактерия делает АТФ, который дальше отправляется хозяину. Хозяин же дает бактерии еду, которую можно превратить в АТФ. Так и живем.
— Вопрос. Дыхание появилось после этой кислородной катастрофы — роста до 20% — или где-то еще? Или это просто неизвестно?
— Вопрос хороший. Дыхание, скорее всего, появилось раньше, потому что помимо кислородного дыхания есть, например, серное дыхание. Можно серу тоже восстанавливать до сероводорода и получать с этого какую-то энергию, делая АТФ. Можно сульфаты восстанавливать до серы с получением энергии. Сернистые соединения были, скорее всего, с начала времен. Дыхание как явление, конечно, появилось раньше, вскоре после появления первых ферментов.
С кислородным дыханием тоже не всё просто. Вот, например, недавно ушедший от нас Владимир Петрович Скулачёв, один из основателей современной биоэнергетики, полагал, что до появления полной дыхательной цепи, обеспечивающей большие количества АТФ, были какие-то ранние простые ферментные системы, которые просто «гасили» этот кислород, превращая его в воду, — было неважно, что при этом не запасалась энергия, важно было не подохнуть. Гораздо проще сделать систему, которая просто уничтожает кислород: ты на этом не зарабатываешь, но ты выживаешь. Это тоже называется дыханием, по-научному это несопряженное дыхание, поскольку оно не сопряжено с синтезом АТФ. Оно есть у многих современных организмов и осуществляется специальными ферментами в случае необходимости. С этим справляется один не очень сложный белковый комплекс. Он просто берет электроны от какого-то доступного ему донора электронов и сбрасывает их на кислород — термодинамически это очень выгодная реакция. Один электронвольт энергии теряется в виде тепла, но зато не надо иметь много очень сложных дыхательных комплексов. Такое дыхание, наверное, тоже появилось до полной дыхательной цепи. А вот бриколаж полной дыхательной цепи происходил уже на фоне кислорода: раз мы не сдохли, давайте мы из этого извлечем что-нибудь полезное по максимуму. Вот такая последовательность событий.
— Теперь скажите, как примерно проинтерпретировать график концентрации кислорода в атмосфере? Насколько я помню, раньше скачка, до 20%, был какой-то плавный подъем, и даже с какими-то зазубринами. Где появился первый кислород? На суше, в каких-нибудь озерах или в море? Или же в бактериальных матах? Где он возник физически, где появились первые, так сказать, признаки кислородной среды?
— Этого мы не знаем и узнать неоткуда: на Земле существует тектоника плит, старые пласты земной коры затягиваются в мантию, очень старых пород нет. Может быть, это была какая-то такая мелководная система, где у вас всего понемножку. Что-то вроде лагун — не буду фантазировать. Пока даже непонятно, у каких бактерий возник кислородный фотосинтез. В связи с появившейся возможностью читать геномы микроорганизмов, которых не удается растить в чистой культуре (это называется метагеномикой), вся микробиология пришла в движение. Количество геномов самых разных организмов выросло на порядки, причем бо́льшую часть этих организмов никто никогда не видел. Не хватает ни рук, ни голов, чтобы в этом разобраться. В частности, нашли, не поверите, в кале австралийских коал какие-то нефотосинтезирующие цианобактерии, прочли их геномы, построили филогенетические деревья, и вышло, что эволюционными предшественниками фотосинтезирующих цианобактерий были какие-то организмы безо всяких следов фотосинтезирующих генов в геномах. То есть какие-то предшественники цианобактерий получили обе фотосистемы от кого-то еще, причем не ясно, была ли у этих фотосистем уже способность разлагать светом кислород или эта способность развилась уже в цианобактериях. Поэтому есть вариант, что способность разлагать воду на свету и выделять кислород возникла в какой-то другой бактериальной группе, а потом перенеслась к предкам цианобактерий — есть такое явление, как перенос генов между микроорганизмами. Легко предположить, что самые первые организмы, научившиеся производить кислород, от него же и погибли, а гены фотосистем перехватили какие-то более устойчивые к кислороду организмы, например те же цианобактерии — они же устойчивы к кислороду.
Другой вариант связан с фотосинтезирующими бактериями из филума Chloroflexota. Это фотосинтезирующие бактерии, которые живут в верхнем слое микробного мата, на открытом свету, т. е. и от сильного света, и от кислорода у них есть какая-то защита. Они живут там же, где и цинобактерии, вперемешку с ними. У них есть ФРЦ второго типа, но не разлагающий воду, очень примитивный. Неделю назад, после четырех лет существования в качестве препринта, в Nature вышла статья 8 про то, что среди этих бактерий нашли организм с ФРЦ типа 1, а также с циклом Кальвина — это цикл биохимических реакций, в котором идет связывание СО2 у зеленых растений. То есть нашлась еще одна группа, у которой вроде бы есть ФРЦ двух типов, правда, не в одном организме, а в разных. Chloroflexota по целому ряду признаков — очень древняя бактериальная группа; может, способность разлагать кислород возникла у них, а потом передалась цианобактериям, рядом с которыми они жили — на суше или на мелководье.
— Давайте пройдемся по временной шкале и повторим то, что мы знаем. Значит, первый фотосинтез, как вы сказали, был около 3 млрд лет назад?
— Нет, он мог быть и раньше — неизвестно когда.
— А первые признаки кислородного фотосинтеза? Или тоже неизвестно?
— Есть разные статьи, кто-то говорит, что 3,8 млрд лет назад, но это всё еще очень мутно. Мне кажется, что каких-то сотен миллионов лет должно было хватить, чтобы всё окислить и начать накапливаться. Ну вот, давайте возьмем 2,7–3 миллиарда.
— Это самое великое кислородное событие произошло где-то два с чем-то миллиарда лет назад, так?
— 2,4–2,5.
— Значит, 500 млн лет до него это уже был кислородный фотосинтез, который как бы подготовил среду, окислив железо…
— Залежам окисленного марганца — 2,7 млрд лет, причем марганец для эволюционной реконструкции важен: каталитический центр, который разлагает воду, представляет собой кластер из четырех атомов марганца и одного атома кальция — очень сложная марганцевая конструкция. И поэтому, когда нашли залежи окисленного марганца возрастом 2,7 млрд лет, говорилось, что, может быть, первые фототрофы, окислившие уже всё железо, стали окислять марганец; при этом у них образовался каталитический центр, в котором связывались эти ионы двухвалентного марганца, и вот они там могли собраться в кластер, который начал окислять воду. Ну вот, окислявшийся 2,7 млрд лет марганец может рассматриваться как промежуточный этап на пути к окислению воды в фотосинтезе.
— У меня вопросы закончились. Не хотите ли что-то сами сказать в заключение? Как бы последнее слово.
— Эта кислородная история, она как бы важная: с одной стороны, мы кислородом дышим, берем энергию, и это очень выгодный процесс, а с другой — кислород все-таки окислитель и изрядная гадость — яд. И поэтому в нашем теле эти вещи как-то вот всё время сбалансированы.
Последнее время я был задействован в каких-то проектах, которые занимались исследованиями этого самого баланса. Какие-то статьи по этому поводу вышли 9 и еще выйдут — это получилось очень интересным. Кислород оказался важен еще в одном отношении. У природы-матушки, на самом деле, много разных задач. И одна из этих задач, о которой Владимир Петрович Скулачёв много говорил в последние годы, — выводить из эволюционного процесса какие-то неудачные варианты. Условно говоря, если организм в популяции заболел, то непонятно, чем он заболел, — может, чем-то заразным. Природа не знает. Поэтому, если ты заболел, то для эволюции лучше, чтобы ты быстрее умер и никого не заразил. И вот эти механизмы сейчас выходят на поверхность. Грубо говоря, есть много сценариев, когда организм заболевает, никакому физическому ущербу не подвергается, а умирает всё равно. Это большая проблема. Спроси́те, от чего умирали люди во время ковида? Мы с коллегами, кстати, заинтересовались этой темой именно в данном контексте. От чего они умерли? Что им вирус сделал плохого? Сам вирус, в общем, ничего плохого сделать не может, а умирали люди, потому что их организм чересчур сильно реагировал на этот незнакомый вирус: начиналась очень сильная иммунная реакция, кровеносные сосуды забивались и человек умирал. Вопрос в том, как запускается эта чрезмерная реакция и как на это можно влиять. Оказалось, что кислород и дыхательная цепь в этом смысле очень важны, потому что через них и запускаются эти чрезмерные реакции организма. Когда наступают какие-то неполадки в организме, дыхательная цепь начинает работать в особом режиме и генерировать активные формы кислорода, которые еще хуже, чем просто кислород. Они окисляют определенные молекулы липидов, и дальше запускается некий каскад, который может привести к смерти. Это важно, потому что это не только ковид, но и сепсис; и многие другие болезни имеют подобную природу, поэтому вот эта игра между нашим организмом и кислородом очень интересна, очень непроста и очень важна для жизни. На самом деле ковид был достаточно сильным стимулом, чтобы начать изучать эти взаимосвязи.
— Да, чрезвычайно актуальная, конечно, тема… Большое спасибо. Давайте на этом и закончим. Еще встретимся, я думаю, в этом же эфире. До свидания!
— Вам спасибо. Да, с удовольствием встретимся еще раз.
1 trv-science.ru/2024/03/koonin-o-proishozhdenii-eukariot
2 Bryant Donald A. (2013). [in: Advances in Botanical Research, vol. 66] Genome Evolution of Photosynthetic Bacteria // Green Bacteria, pp. 99–150.
3 Kuang T. et al. Architecture of the photosynthetic complex from a green sulfur bacterium // Science, 370 (6519), eabb6350.
4 Mulkidjanian A. Y., Galperin M. Y., Koonin E. V. Co-evolution of primordial membranes and membrane proteins // Trends Biochem Sci 34(4) (2009) 206–15.
Dibrova D. V., Cherepanov D. A., Galperin M. Y., Skulachev V. P., Mulkidjanian A. Y. Evolution of cytochrome bc complexes: from membrane-anchored dehydrogenases of ancient bacteria to triggers of apoptosis in vertebrates // Biochim Biophys Acta 1827(11–12) (2013) 1407–27.
Dibrova D. V., Shalaeva D. N., Galperin M. Y., Mulkidjanian A. Y., Emergence of cytochrome bc complexes in the context of photosynthesis // Physiol Plant 161(1) (2017) 150–170.
5 Glass J. B., Elbon C. E., Williams L. D. Something old, something new, something borrowed, something blue: the anaerobic microbial ancestry of aerobic respiration // Trends Microbiol 31(2) (2023) 135–141.
6 Bricolage — процесс преобразования значения объектов или символов посредством нового использования или нестандартных переделок несвязанных вещей (Дэвид Джери, Джулия Джери. Большой толковый социологический словарь. — М.: АСТ, Вече,1999).
7 Darbani B., Kell D. B., Borodina I. Energetic evolution of cellular Transportomes // BMC Genomics 19(1) (2018) 418.
8 Tsuji J. M., Shaw N. A., Nagashima S., Venkiteswaran J. J., Schiff S. L., Watanabe T., Fukui M., Hanada S., Tank M., Neufeld J. D. Anoxygenic phototroph of the Chloroflexota uses a type I reaction centre // Nature (2024)
9 Chernyak B. V., Lyamzaev K. G., Mulkidjanian A. Y. Innate Immunity as an Executor of the Programmed Death of Individual Organisms for the Benefit of the Entire Population // Int J Mol Sci 22(24) (2021).
Skulachev V. P., Vyssokikh M. Y., Chernyak B. V., Mulkidjanian A. Y., Skulachev M. V., Shilovsky G. A., Lyamzaev K. G., Borisov V. B., Severin F. F., Sadovnichii V. A. Six Functions of Respiration: Isn’t It Time to Take Control over ROS Production in Mitochondria, and Aging Along with It? // Int J Mol Sci 24(16) (2023).


 (5 оценок, среднее: 4,80 из 5)
(5 оценок, среднее: 4,80 из 5)
Прекрасная статья, много интересных мыслей. Размышления о том что иммунитет по определению популяционный и одна из задач иммунной системы убить больного, чтобы он не заразил остальных, в последнее время активно обсуждается нами.
А вот система несопряженного дыхания, не могла ли она быть первичной т.е. тепло этот тоже энергия и локальный нагрев бактериальной клетки ускоряет химические реакции, что эволюционно выгодно само по себе?
В статье «интересная мысль» сформулирована довольно экстравагантно:
А по мне, более интересна формулировка из «Белого солнца пустыни»:
— Тебя как, сразу кончить, или желаешь помучиться?
— Лучше, конечно, помучиться.
если поразмышлять о цитокиновом шторме и иммуноопосредованных повреждениях организма при инфекции, то это так и выглядит — если темпы инфекционного процесса слишком велики то активация ряда параллельных провоспалительных каскадов регуляции позволяет поставить вопрос ребром — или ты выживаешь в условиях максимальной активации иммунной системы или ты погибаешь, переставая выделять других. Однако более ценные женщины и дети менее подвержены такому типу воздействия (вспомним ковид) в сравнении с пожилыми людьми и мужчинами…. Если есть апоптоз при вирусных инфекциях и он работает, то почему бы не быть его функциональному аналогу на популяционном уровне?
”это так и выглядит”
Может быть, однако когда армия освобождает город от врагов, это тоже выглядит как его уничтожение, хотя далеко не факт, что ей была поставлена именно такая задача ”убить город”. Исход болезни это некий компромисс, между воздействием патогенов и иммунитета на организм, и его способности (и воли) к дальнейшему существованию. Если больной считает, что ”Лучше, конечно, помучиться”, то для популяции и эволюции он ещё не потерян, а за одного битого двух небитых дают. Переболевший имеет рабочие опробованные механизмы борьбы с заразой, которые он может передать популяции. Так что, далеко не очевидно, что именно в конечном итоге ”лучше для эволюции”.
есть сложность баланса между чувствительностью системы элиминирующей неудачные варианты иммунной системы и риском настолько сузить бутылочное горлышко, что популяция не пролезет… Так как цитокиновый шторм, как популяционный вариант апоптоза, все же меньше затрагивает женщин т.е. санитарный эффект явно не идеален, то скорее все же важна именно гибель части особей. Но и Treg клетки (подавляющие и воспаление и снижающие напряженность адаптивного иммунитета) накапливаются небыстро т.е. если помучится достаточно долго, то мы приходим к хронической инфекции… Эволюционные выгоды от хронической инфекции и бессимптомного носительства тоже есть. Впрочем, тут еще важно какова численность вида и объем лимфоидной ткани у особи, в среднем.
Естественно, санитарный (как и любой другой) эффект не идеален, и гибель части особей может быть даже необходима, но далеко не так однозначно-категорично, как в процитированной мною фразе из статьи ;)
Да. Конечно. Какая то часть популяции должна погибать или выключатся из размножения т.к. это обеспечивает отбор. Если старение эволюционно-выгодно, то и гибель части популяции от неблагоприятных факторов тоже эволюционно-выгодно само по себе (для массовых видов). Пожалуй должны быть разного рода флюктуации выносливости у индивида, чтобы часть генетически идентичных особей могла погибнуть, но не вся. Инфекции тут выглядят очень удобным инструментом. А есть еще половой отбор и в нем тоже инфекции порой могут вносить вклад
Вроде там и говорится, что она первична.
я имел ввиду что первична не для защиты от кислорода а первична для получения тепловой энергии? То есть жизнь могла в принципе начаться на тепловой энергии.
«Как бы последнее слово»
Не испугает только больного
Способного к самокремации
Ради эволюции популяции…
Эволюционным Иммунитетом объявлен врагом популяции, и именем эволюции приговорён к аннигиляции.
Помнится мне, должно было быть сделано ещё одно важное изобретение — деление клетки на две такие же. Говорят, его придумали вирусы? Оно должно было предшествовать всем прочим гибридизациям?
Почему-то эта тема пропущена. Либо тут науке всё понятно и неинтересно, либо не известно вообще ничего и рассказать не о чём?
думаю да. Я вообще считаю, что многоклеточность предшествовала способности одной автономной клетки породить такую же
Логарифмический масштаб кислородной оси на первом рисунке акцентирует внимание читателя на лаг-фазе роста кислорода в земной биосфере.
Я оцифровал рисунок и перестроил его так, чтобы на нем были логарифмическая и привычная линейная шкала кислородной оси. Тогда читателю видно, — экспоненциальная фаза роста кислорода закончилась.
Экспоненциальную фазу имитировал моделью роста клеток бинарным делением с временем генерации 95 млн земных лет, — это близко к оценке по формуле:
(постоянная тонкой структуры)/(параметр Хаббла)=105 млн лет.
Похоже, впереди либо кислородное плато, либо, — в соответствии со сказкой Ханнеса Альвена, — спад, — ведь миру самовоспроизводящихся суперкомпьютеров кислород не очень-то и нужен. ))