
Присуждение Нобелевской премии по химии 2014 года комментирует Андрей Наумов, докт. физ.-мат. наук, Институт спектроскопии РАН (Троицк), Московский педагогический государственный университет (Москва), www.isan.troitsk.ru/~naumov
Нобелевская премия по химии 2014 года присуждена Уильяму Мёрнеру (Стэнфордский университет, США), Эрику Бетцигу (Медицинский институт Говарда Хьюза, США) и Штефану Хеллю (Институт Макса Планка в Гейдельберге, Германия) за развитие методов флуоресцентной микроскопии сверхвысокого разрешения.
Оптическая микроскопия принадлежит к числу старейших экспериментальных методов, сохранивших свою высокую значимость во многих научных дисциплинах. Начиная с работы Аббе 1873 года [1] стало ясно, что пространственное разрешение дальнеполевого микроскопа, основанного на фокусирующей оптике, имеет предел, который определяется дифракцией и составляет примерно 1/2 длины волны регистрируемого излучения (т.е. в видимой области спектра ~200–300 нм).
Конечно, к настоящему времени разработан целый ряд методов, позволяющих восстановить субдифракционную структуру материала: электронная, атомно-силовая, ближнеполевая сканирующая, рентгеновская микроскопия… Однако каждый из этих методов обладает принципиальными недостатками, затрудняющими их широкое использование для нанодиагностики структуры и динамики образцов, особенно в тех случаях, когда речь идет об оперативности исследования, простоте процедуры измерения, необходимости диагностики структуры и динамики объекта, его поверхности и объема.
Развитие методов лазерной флуоресцентной микроскопии позволило исследователям преодолеть (именно преодолеть, а не «отменить») классический дифракционный предел в оптической микроскопии.
Одиночные молекулы
Первая группа методов оптической «наноскопии» основана на детектировании одиночных флуоресцирующих молекул. Для реализации этой идеи нужно добиться раздельного (селективного) детектирования отдельных молекул, т. е. перейти от регистрации одновременного свечения огромного ансамбля молекул к предельно малым концентрациям и далее к одиночным молекулам (ОМ).
Здесь нужно отметить основополагающий вклад отечественных ученых в развитие спектроскопии органических молекул. Активные работы по изучению люминесценции растворов проводились в лаборатории люминесценции ФИАН под руководством С. И. Вавилова, а в 1952 году сотрудники кафедры теоретической физики Московского государственного педагогического института под руководством Э.В. Шпольского впервые наблюдали эффект возникновения квазилинейчатых спектров сложных органических соединений в специально подобранных растворителях при низких температурах. При криогенных температурах спектры внедренных молекул, жестко зафиксированных в прозрачных матрицах, становятся очень узкими. Тогда появляется возможность возбуждать, заставлять светиться не все молекулы, а их отдельные ансамбли. В 1972 году ученик Шпольского профессор Р.И. Персонов с коллегами добились в Институте спектроскопии АН СССР успеха по селективному лазерному возбуждению свечения органических молекул. Затем в 1974 году лаборатория Персонова и его коллеги из Института физики в Тарту провели пионерские опыты по «выжиганию спектральных провалов», когда с помощью лазера часть молекул «переводилась в безызлучательное состояние», не светилась. Эти работы легли в основу направления селективной лазерной спектроскопии молекул, кульминационным достижением которого стала спектроскопия одиночных молекул (СОМ) [2].
В 1989 году У. Мёрнер и Л. Кадор продемонстрировали возможность регистрации спектров поглощения ОМ [3], а спустя всего несколько месяцев М. Оррит и Дж. Бернард убедительно доказали в эксперименте возможность детектирования флуоресцентного свечения ОМ в твердой матрице при криогенных температурах [4]. За 25 лет, прошедших с первых экспериментов, данное направление интенсивно развивалось и стало одним из наиболее актуальных в физической химии, биофизике и смежных науках. Всё возрастающий интерес к СОМ обусловлен рядом причин:
- Физико-химические свойства вещества могут быть исследованы на минимально возможном уровне — на уровне отдельных молекул.
- Оптические спектры и спектральная динамика ОМ, внедренных в изучаемую среду (жидкость, твердое тело) в качестве нанозондов, содержат беспрецедентно богатую информацию как о самих излучателях, так и о параметрах ближайшего окружения.
- Регистрация люминесцентных изображений одиночных точечных излучателей в схеме сканирующего конфокального микроскопа или классического люминесцентного микроскопа с 2D-детектором позволяет реконструировать координаты ОМ с субдифракционной (нанометровой) точностью.
Микроскопия с реконструкцией изображений одиночных молекул
Фотоны люминесценции ОМ формируют на 2D-детекторе изображение точечного источника света. Анализ изображения ОМ с учетом определенной формы аппаратной функции точечного источника позволяет определить положение (координаты) ОМ с погрешностью, которая ограничена только стабильностью установки, отношением «сигнал — шум» регистрируемого излучения и размерами самого точечного источника, и может существенно превосходить дифракционный предел (рис. 1).
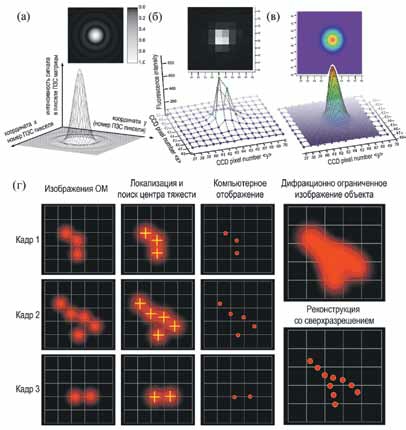
В то же время задачи диагностики протяженных объектов, как правило, требуют детектирования значительного количества ОМ и их высокой пространственной плотности. В этом случае одновременное свечение тысяч молекул не позволяет различить изображения одиночных точечных источников — идентификация и определение точных положений ОМ становятся невозможными. Обойти это затруднение возможно, если разные ОМ излучают в разные моменты времени, либо различая ОМ, находящиеся внутри общего дифракционного предела по дополнительному признаку или свойству [5].
Существует несколько методов, позволяющих реализовать эту идею. Наибольшее распространение к настоящему времени получила техника, в основе которой лежит явление мерцания флуоресценции одиночных квантовых объектов. Случайное прерывание флуоресценции отдельных молекул происходит в разные моменты времени. Таким образом, при достаточно низкой концентрации примесных молекул в каждый момент времени внутри каждого дифракционно ограниченного объема образца люминесцирует только одна молекула, что и позволяет зарегистрировать ее изображение и, как следствие, координаты. Эта идея была реализована в технике photoactivation localization microscopy (PALM) коллективом под руководством Э. Бетцига [6]. Следует отметить, что примерно в это же время успешно развивалась основанная на тех же принципах техника stochastic optical reconstruction microscopy (STORM) [7]. В самые последние годы были разработаны оригинальные методы визуализации ОМ, которые позволяют определять с нанометровой точностью все три координаты точечного излучателя [8, 9].
Микроскопия с подавлением спонтанного излучения
Параллельно с «одномолекулярными» методиками в середине 2000-х успешно развивалась вторая группа методов оптической наноскопии, основанных на манипулировании с параметрами возбуждающего излучения и нелинейным откликом исследуемой среды. Специфический подбор параметров возбуждающего лазерного излучения позволяет существенно уменьшить характерные размеры аппаратной функции микроскопа. В частности, в разработанной Ш.Хеллем технике stimulated emission depletion (STED) [5], эффективный объем материала, из которого регистрируется флуоресценция, уменьшается за счет перевода в безызлучательное (на рабочей длине волны) состояние части молекул по краям пятна засветки сфокусированного лазерного излучения. Обеднение флуоресценции достигается за счет второго лазера с заданным поперечным профилем пучка. В данном случае приходится использовать технику сканирующей конфокальной микроскопии, однако базис техники всё тот же — в случае, когда регистрируется излучение от агломерации молекул с размерами, существенно меньше длины волны света, возможно определение координат этой группы молекул с субдифракционной точностью.
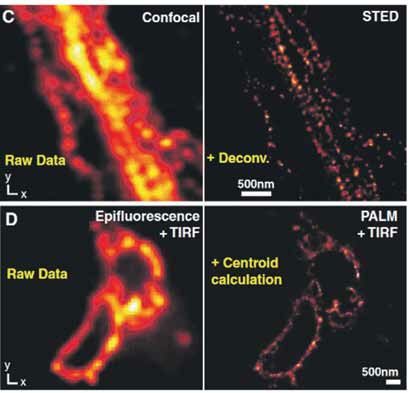
Применения и перспективы
На основе методов STED, PALM, STORM были созданы первые коммерческие оптические «наноскопы» — микроскопы сверхвысокого разрешения, оборудованные лазерными источниками, ультрачувствительными детекторами и мощными компьютерами, которые позволяют быстро распознавать и восстанавливать изображения. Разработанные методы и инструменты уже оказались широко востребованы в биохимии, биофизике и смежных науках, а также открывают новые перспективы в области наносенсорики, медицинской физики, материаловедения, квантовой оптики и нанотехнологий (см. статью-коллоквиум [9]). В этой связи есть все основания полагать, что Нобелевская премия 2014 года — далеко не последняя в череде ярких подтверждений потенциала этого направления науки.
1. Abbe, Beiträge zur Theorie des Mikroskops und der mikroskopischen Wahrnehmung // Archiv für Mikroskopische Anatomie, 9 (1), 413-418 (1873).
2. А.В. Наумов, «Спектроскопия органических молекул в твёрдых матрицах при низких температурах: от эффекта Шпольского к лазерной люминесцентной спектромикроскопии всех эффективно излучающих одиночных молекул» // Успехи Физических Наук, 183 (6), 633-652 (2013).
3. E. Moerner, L. Kador, Optical-Detection and Spectroscopy of Single Molecules in a Solid // Physical Review Letters, 62 (21), 2535-2538 (1989).
4. Orrit, J. Bernard, Single pentacene molecules detected by fuorescence excitation in para-terphenyl crystal // Physical Review Letters, 65 (21), 2716-2719 (1990).
5. W. Hell, Far-feld optical nanoscopy // Science, 316 (5828), 1153-1158 (2007).
6. E. Betzig, G.H. Patterson, R. Sougrat, O.W. Lindwasser, S. Olenych, J.S. Bonifacino, M.W. Davidson, J. Lippincott-Schwartz, H.F. Hess, Imaging intracellular fuorescent proteins at nanometer resolution // Science, 313 (5793), 1642-1645 (2006).
7. J. Rust, M. Bates, X.W. Zhuang, Sub-diffraction-limit imaging by stochastic optical reconstruction microscopy (STORM) // Nature Methods, 3 (10), 793-795 (2006).
8. R.P. Pavani, M.A. Thompson, J.S. Biteen, S.J. Lord, N. Liu, R.J. Twieg, R. Piestun, W.E. Moerner, Three-dimensional, single-molecule fuorescence imaging beyond the diffraction limit by using a double-helix point spread function // Proceedings of the National Academy of Sciences of the United States of America, 106 (9), 2995-2999 (2009).
9. V. Naumov, I.Y. Eremchev, A.A. Gorshelev, Laser Selective Spectromicroscopy of Myriad Single Molecules: Tool for Far-Field Multicolor Materials Nanodiagnostics // European Physical Journal D, Colloquium paper (in print) DOI: 10.1140/epjd/e2014-50414-x (2014).

Добрый день! Тема раскрыта лишь частично. Полностью отсутствует критическая оценка методов. Прежде всего, оба метода требуют значительного времени на построение одного изображения — следовательно не пригодны для изучения динамики одиночных молекул в живых клетках, многие события на уровне отдельных молекул происходят за доли секунды. Чаще всего примеры применения PALM и STORM ограничены реконструкцией сети микротрубочек — именно из медленной динамики этих структур. Потому то автор и не смог ничего сказать в разделе «Применения и перспективы». Кроме описанных методов существуют другие методы прижизненной микроскопии одиночных молекул, которые позволяют определять движущихся молекул с точностью 5-20нм.
С уважением
Григорий Машанов
Ну вот как только эти методы получат Нобелевскую премию, так и про них можно будет написать :-)